Osakeste lainelised omadused. Laadige alla raamat "Üldine ja anorgaaniline keemia" (5,36Mb) Millistel järgmistest osakestest on lainelised omadused
Kvantmehaanika on kaasaegne teooria, mis kehtestab kirjeldusmeetodi ja mikroosakeste liikumisseadused ( elementaarosakesed, aatomid, molekulid, tuumad) ja nende süsteemid. Kvantmehaaniliste kontseptsioonide ebatavalisus võrreldes klassikalise füüsikaga avas füüsikaliste põhimudelite murdmise perioodi, mis tundus ilmselge ja hävimatu. See puudutas peamiselt osakese mõistet ja selle liikumise põhimõtteid.
See peatükk annab kontseptsiooni mitte ainult kvantmehaanika kohta, vaid ka nende ideede ja katsete kohta, mis selle teooriani viisid. Elektronmikroskoopiat peetakse meetodiks, mis põhineb elektronide laineomadustel.
28.1. DE BROYLE'I HÜPOTEES. ELEKTRONIDE JA MUUD OSAKESTE DIFRAKTSIOONIDE KATSED
Oluline samm kvantmehaanika loomisel oli mikroosakeste laineomaduste avastamine. Laineomaduste idee esitas algselt hüpoteesina prantsuse füüsik Louis de Broglie (1924) 1 .
Füüsikas domineeris aastaid teooria, mille kohaselt on valgus elektromagnetlaine. Pärast Plancki (soojuskiirgus), Einsteini (fotoelektriline efekt) jt tööd sai aga selgeks, et valgusel on korpuskulaarsed omadused.
1 De Broglie hüpotees püstitati enne osakeste lainelisi omadusi kinnitavaid katseid. De Broglie kirjutas sellest hiljem, 1936. aastal, järgmiselt: „... kas me ei saa eeldada, et elektron on sama duaalne kui valgus? Esmapilgul tundus see idee väga julge. Lõppude lõpuks oleme elektroni alati ette kujutanud elektriliselt laetuna materiaalne punkt, mis järgib klassikalise dünaamika seadusi. Elektron ei ole kunagi selgelt avaldanud selliseid laineomadusi, nagu näiteks valgus interferentsi ja difraktsiooni nähtustes. Katse omistada elektronidele laineomadusi, kui selle kohta puuduvad eksperimentaalsed tõendid, võib tunduda ebateadusliku fantaasiana.
Peatükis 24 märgiti, et röntgenikiirguse difraktsiooni täheldatakse kristallkehadel; seetõttu tuleb elektronide difraktsiooniks kasutada ka kristalseid aineid.
K. Davisson ja L. Germer olid esimesed, kes jälgisid elektronide difraktsiooni nikli üksikkristallil, J.P. Thomson ja temast sõltumatult P.S. Tartakovski - metallfooliumil (polükristalliline keha).
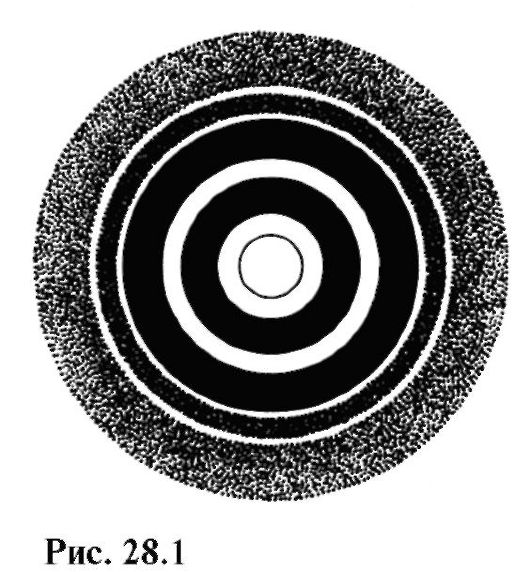
Joonisel fig. 28.1 näitab elektrongrammi – difraktsioonimustrit, mis saadakse elektronide interaktsioonist polükristallilise fooliumiga.
Võrreldes seda joonist joonisega fig. 24.21, võib märgata elektronide ja röntgendifraktsiooni sarnasust.
Ka teistel osakestel on difraktsioonivõime, nii laetud (prootonid, ioonid jne) kui ka neutraalsed (neutronid, aatomid, molekulid).
Sarnaselt röntgendifraktsioonianalüüsile saab osakeste difraktsiooni abil määrata aine aatomite ja molekulide järjestatud või ebakorrektset paigutust ning hinnata kristallvõrede parameetreid.
Praegu kasutatakse laialdaselt elektronide difraktsiooni (elektronide difraktsiooni) ja neutronite difraktsiooni (neutronide difraktsiooni) meetodeid.
Võib tekkida küsimusi: mis saab üksikutest osakestest, kuidas kujunevad maksimumid ja miinimumid üksikute osakeste difraktsiooni käigus?
Väga madala intensiivsusega elektronkiirte difraktsiooni katsed, s.o. justkui eraldiseisvad osakesed, näitas, et sel juhul ei "määrdu" elektron eri suundades, vaid käitub nagu terve osake. Samas on difraktsiooniobjektiga interaktsiooni tulemusena elektronide läbipainde tõenäosus erinevates suundades erinev. Elektronid tabavad kõige tõenäolisemalt kohti, mis arvutuse järgi vastavad difraktsioonimaksimumidele, nende tabamine miinimumidele on väiksem. Seega on laineomadused omased mitte ainult elektronide kollektiivile, vaid ka igale elektronile eraldi.
28.2. ELEKTRONMIKROSKOOP. ELEKTROONIKA OPTIKA MÕISTE
Osakeste laineomadusi saab kasutada mitte ainult difraktsioonistruktuuri analüüsiks, vaid ka objektist suurendatud kujutiste saamiseks.
(26.19) järeldub, et optilise mikroskoobi eraldusvõime piiri määrab peamiselt inimsilma poolt tajutava valguse lainepikkuse piirväärtus. Asendades selles valemis de Broglie lainepikkuse väärtuse (28,3), leiame elektronmikroskoobi eraldusvõime piiri, milles objekti kujutise moodustavad elektronkiired:
On lihtne näha, et eraldusvõime piir z elektronmikroskoop sõltub kiirenduspingest ja on võimalik saavutada, et see on palju väiksem ja eraldusvõime on palju suurem kui optilisel mikroskoobil.
Elektronmikroskoop ja selle üksikud elemendid on oma eesmärgi poolest sarnased optilise mikroskoobiga, seega kasutame selle struktuuri ja tööpõhimõtte selgitamiseks analoogiat. Mõlema mikroskoobi diagrammid on näidatud joonisel fig. 28,2 (a - optiline; b - elektrooniline).
Optilises mikroskoobis objekti kohta teabe kandja AB on footon, valgus. Valgusallikaks on tavaliselt hõõglamp /. Pärast interaktsiooni objektiga (neeldumine, hajumine, difraktsioon) muundub footoni voog ja see sisaldab teavet objekti kohta. Footonivoo moodustamiseks kasutatakse optilisi seadmeid, peamiselt läätsi: kondensaator 3, objektiiv 4, okulaar 5. Pilt A 1 B 1 salvestatakse silmaga 7 (või fotoplaadiga, fotoluminestsentsekraaniga jne).
Elektronmikroskoobis on objekti kohta teabe kandjaks elektron ja elektronide allikaks kuumutatud katood 1. Elektronide kiirendamine ja kiire moodustumine toimub fokusseeriva elektroodi ja anood - süsteemi abil. nimetatakse elektronkahuriks 2. Pärast objektiga suhtlemist (peamiselt hajumist) muundub elektronvoog ja see sisaldab teavet subjekti kohta. Elektronvoo moodustumine toimub elektrivälja (elektroodide ja kondensaatorite süsteem) ja magnetvälja (süsteem) mõjul

ma mähised vooluga). Neid süsteeme nimetatakse elektroonilisteks läätsedeks analoogselt optiliste läätsedega, mis moodustavad valgusvoo. (3 - kondensaator; 4 - elektrooniline, toimib objektiivina, 5 - projektsioon). Kujutis salvestatakse elektronitundlikule fotoplaadile või katodoluminestsentsekraanile 6.
Elektronmikroskoobi eraldusvõime piiri hindamiseks asendame valemiga (28.4) kiirenduspinge 100 kV ja nurkava suurusjärgus 10 -2 rad (ligikaudu selliseid nurki kasutatakse elektronmikroskoopias). Siis saame z ~ 0,1 nm, mis on sadu kordi parem kui optilised mikroskoobid. Suurema kui 100 kV kiirenduspinge kasutamine, kuigi see suurendab eraldusvõimet, on seotud teatud raskustega, eriti esineb see
uuritava objekti hävitamine suure kiirusega elektronide poolt. Praktikas võib isegi parima elektronmikroskoobiga saavutada eraldusvõime piiri suurusjärgus 10-10 m; see on sadu kordi parem kui optilised mikroskoobid.
Elektronmikroskoobi eelisteks on kõrge eraldusvõime, mis võimaldab arvestada suurte molekulidega, võime vajadusel muuta kiirenduspinget ja sellest tulenevalt ka eraldusvõime piiri ning elektronide voolu suhteliselt mugav juhtimine magneti abil. ja elektriväljad.
Toome välja mõned elektronmikroskoobi töö omadused. Nendes osades, kus elektronid lendavad, peab olema vaakum, kuna vastasel juhul põhjustab elektronide kokkupõrge õhu (gaasi) molekulidega pildi moonutamist. See elektronmikroskoopia nõue muudab uurimisprotseduuri keerulisemaks, muudab seadmed tülikamaks ja kallimaks. Vaakum moonutab bioloogiliste objektide loomulikke omadusi ja mõnel juhul hävitab või deformeerib neid.
Elektronmikroskoobis vaatamiseks sobivad ainult väga õhukesed lõigud, kuna aine neeldub ja hajutab elektronid tugevalt. Seetõttu on mõnel juhul soovitatav teha objekti uuritavast pinnast jäljend õhukesele plastikukihile. Seda protseduuri nimetatakse replikatsiooniks ja pinna plastiliseks koopiaks koopia.

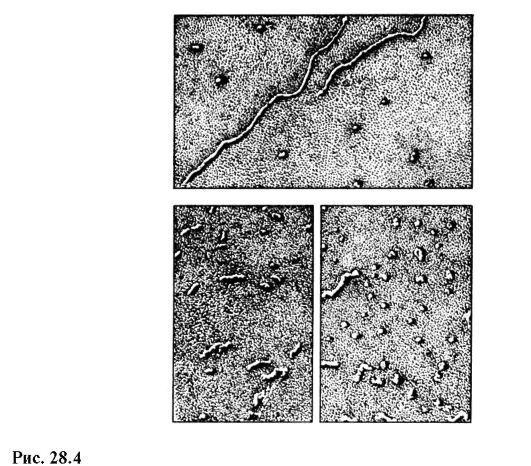
Kaasaegne kodumaine elektrooniline mikroskoop EVM-100 LM (joon. 28.3) annab maksimaalseks suurenduseks 600 000 korda ja garanteeritud eraldusvõime piiriks 3? 10 -10 m. Joonisel fig. 28.4 näitab erinevates olekutes olevaid RNA molekulide pilte, mis on saadud elektronmikroskoobiga 100 000-kordse suurendusega.
Nii footonite kui ka elektronide ja muude osakeste laine- ja korpuskulaarsete omaduste olemasolu võimaldab laiendada mitmeid optika sätteid ja seadusi, et kirjeldada laetud osakeste liikumist elektri- ja magnetväljas.
See analoogia võimaldas eraldi sektsioonina välja tuua elektrooniline optika - füüsika valdkond, milles laetud osakeste kiirte struktuur interakteeruvad elektri- ja magnetväljad. Sarnaselt tavalise optikaga saab elektroonika jagada järgmisteks osadeks geomeetriline (tala) ja Laine(füüsiline).
Geomeetrilise elektronoptika raames kirjeldatakse eelkõige laetud osakeste liikumist elektri- ja magnetväljas. Pildistamise skemaatiline esitus elektronmikroskoobis (vt joonis 28.2, b) põhineb geomeetrilisel elektronoptikal.
Laineelektronoptika lähenemine on oluline juhul, kui avalduvad laetud osakeste laineomadused. Hea näide on lõigu alguses toodud eraldusvõime (eraldusvõime piirangu) leidmine.
28.3. LAINFUNKTSIOON JA SELLE FÜÜSIKALINE TÄHEND
Kuna mikroosake seostatakse tema liikumisele vastava laineprotsessiga, kirjeldab osakeste olekut kvantmehaanikas koordinaatidest ja ajast sõltuva lainefunktsiooniga: ψ(χ, y, z, t).
Kui osakesele mõjuv jõuväli on statsionaarne, s.o. sõltumatult ajast, siis saab ψ-funktsiooni esitada kahe teguri korrutisena, millest üks sõltub ajast ja teine koordinaatidest:
Järgnevalt käsitleme ainult statsionaarseid olekuid; Funktsioon ψ on osakese oleku tõenäosustunnus. Selgitame selle väite tähendust.
Eraldagem ruumis piisavalt väike maht dV= dxdjdz, mille piires võib ψ-funktsiooni väärtusi pidada samaks. Leidmise tõenäosus dW B osakeste sisaldus selles ruumalas on võrdeline ruumalaga ja sõltub ψ-funktsiooni mooduli ruudust:

Lainefunktsiooni mooduli ruut on võrdne tõenäosustihedusega, s.o. ruumalas oleva osakese leidmise tõenäosuse ja selle ruumala suhe.
Integreerides avaldise (28.6) mõne ruumala V peale, leiame tõenäosuse leida selles mahus osake:
28.4. MÄÄRAMUSSUHTED
Üks kvantmehaanika olulisi sätteid on W. Heisenbergi pakutud määramatuse suhted.
Mõõdetakse osakese asendit ja impulssi üheaegselt, kusjuures abstsissi definitsioonide ja impulsi projektsiooni abstsissteljele on ebatäpsused vastavalt Δχ ja Δр x.

1 Sellist katset on tõesti võimatu läbi viia, kuna pilu mõõtmed peavad olema aatomite suurusjärgus, seetõttu kirjeldatakse mõnda vaimset eksperimenti.
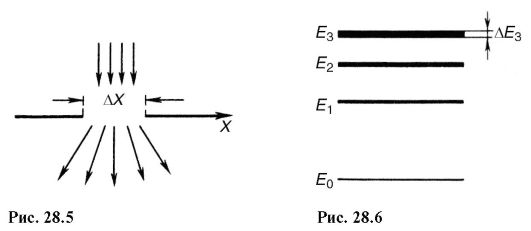
Lahendus (28.11) tähendab, et mida lühem on süsteemi mis tahes oleku eksisteerimise aeg, seda ebakindlam on selle energia väärtus. Energiatasemed E 1 , E 2 jne. olema teatud laiusega (joonis 28.6), olenevalt ajast, mil süsteem on sellele tasemele vastavas olekus.
Taseme "hägunemine" toob kaasa emiteeritud footoni energia AE ja selle sageduse Ay määramatuse süsteemi üleminekul ühelt energiatasemelt teisele:
Kuna mikroosakese olekut kirjeldab ψ-funktsioon, siis tuleb välistingimusi arvestades ära näidata selle funktsiooni leidmise meetod. See on võimalik E. Schrödingeri (1926) pakutud kvantmehaanika põhivõrrandi lahendamise tulemusena. Selline võrrand kvantmehaanikas on postuleeritud samamoodi nagu klassikaline mehaanika Newtoni teine seadus on postuleeritud.
Statsionaarsete olekute puhul saab Schrödingeri võrrandi kirjutada järgmiselt:
See väljendub spektrijoonte laienemises.
28.5. SCHROEDINGERI VÕRD. ELEKTRON POTENTSIAALSES KAEVUS
kus m- osakeste mass; E ja E p on selle kogu- ja potentsiaalne energia (potentsiaalse energia määrab jõuväli, milles osake asub, ja statsionaarsel juhul ei sõltu see ajast).
Kui osake liigub ainult mööda mingit joont, näiteks piki telge X(ühemõõtmeline juhtum), siis on Schrödingeri võrrand oluliselt lihtsustatud ja võtab järgmise kuju:
Üks kõige enam lihtsaid näiteid Schrödingeri võrrandi kasutamise kohta on ühemõõtmelises potentsiaalikaevus osakese liikumise ülesande lahendus.
Laske elektronil liikuda mööda telge X ainult 0 piires< X < l(Joon. 28.7). See tähendab, et näidatud intervallis on ψ-funktsioon nullist erinev ja väljaspool intervalli (x<0, X>l) on võrdne nulliga.
Kuna jõuväljad ei mõju osakesele valitud intervallis, võib selle potentsiaalsel energial olla mis tahes konstantne väärtus (kõige mugavam on võtta E lk= 0). Väljaspool seda intervalli pole elektrone, seega tuleks selle potentsiaalset energiat pidada lõpmatult suureks. Joonisel fig. 28.7 näitab E p \u003d D x) graafilist sõltuvust. Intervall 0< X < l, удовлетворяющий сформулированным выше условиям, называют одномерной прямоугольной потенциальной ямой с бесконечно высокими стенками. С учетом E lk= 0 Schrödingeri võrrand (28.14) intervalli 0 jaoks< X < l tundub, et:

See võrrand on sarnane diferentsiaalvõrrand harmooniline võnkumine (vt 7.1), mille lahendus on:

Esiteks on tähelepanuväärne, et Schrödingeri võrrandi lahendamine potentsiaalikaevu elektroni jaoks ilma täiendavate postulaatideta viib diskreetsete, kvantiseeritud energiaväärtusteni:

Alates (28.21) on näha, et mõne fikseeritud väärtuse puhul n diskreetsus, s.t. naabertasandite energiate erinevus on seda väiksem, seda suurem on potentsiaalikaevu suurus. Mõelge näiteks kahele juhtumile n = 1:
1) l= 5? 10-10 m, mis vastab ligikaudu aatomi suurusele; siis ΔΕ = 4,5 eV. See langeb suurusjärgus kokku Bohri teooria järgi vesinikuaatomi jaoks saadud väärtustega;
2) l= 10 -1 m, mis tegelikult vastab sellisele potentsiaalikaevu laiusele, et elektroni võib lugeda vabaks; kus ΔΕ = 1.1? 10 -16 eV. Siin on diskreetsus tühine ja praktiliselt võib arvata, et elektronide energia muutub pidevalt.
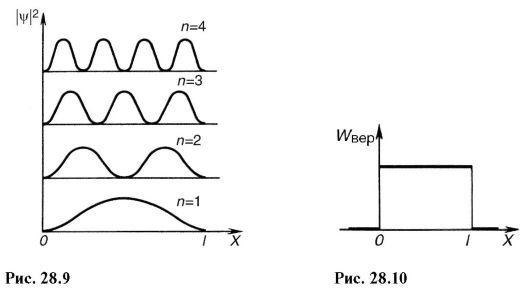
Kvadrutades (28.20) saame tõenäosustiheduse |ψ| 2 elektroni leidmine sisse erinevad punktid potentsiaalne kaev. Joonisel fig. 28.9 näitab graafiline sõltuvus|ψ| 2 maha χ erinevates diskreetsetes olekutes, st. erinevad kvantarvud. Nagu jooniselt näha, võib elektron olla potentsiaalikaevu erinevates kohtades erineva tõenäosusega. On punkte, kus elektroni leidmise tõenäosus on üldiselt võrdne nulliga. See erineb oluliselt klassikalise füüsika ideedest, mille kohaselt on võrdselt tõenäoline, et osake asub potentsiaalikaevu erinevates kohtades (joon. 28.10) ning kaevu on võimatu jagada punktidega, milles on võimalik kaevu olemasolu. osake on välistatud.
Schrödingeri võrrandit saab rakendada ka keerukamatele jõuväljadele, näiteks elektronile aatomis. See toob kaasa täiendavaid matemaatilisi raskusi, kuid ei muuda põhifunktsioone.
aatomisüsteemid: energiaseisundite diskreetsus, tõenäosuslikud hinnangud elektroni leidmise kohta, omamoodi sõltuvus |ψ| 2 koordinaatidelt jne.
28.6. SCHROEDINGERI VÕRDLUSE RAKENDAMINE VESINIKUAatomiLE. KVANTNUMBRID
Aatomite ja molekulide olekute kirjeldamine Schrödingeri võrrandi abil on üsna keeruline ülesanne. Kõige lihtsam on see lahendada ühe elektroni puhul, mis asub tuuma väljas. Sellised süsteemid vastavad vesinikuaatomile ja vesinikulaadsetele ioonidele (üksikioniseeritud heeliumiaatom, topeltioniseeritud liitiumiaatom jne). Kuid ka sel juhul jääb probleemi lahendamine meie kursuse raamidest välja, seega piirdume probleemi kvalitatiivse esitlemisega.
Esiteks tuleks potentsiaalne energia asendada Schrödingeri võrrandiga (28.13), mis kahe interakteeruva punktitasud - e(elektron) ja Ze(tuum), - asub kaugusel r vaakumis väljendatakse järgmiselt:
Tuuma poolt tekitatava välja kesksümmeetriaga on mugavam ülesannet lahendada mitte ristkülikukujuliste koordinaatide, vaid sfääriliste r, θ ja p järgi.
Schrödingeri võrrandi lahendus leitakse kolme funktsiooni korrutisena, millest igaüks sõltub ühest muutujast:
Nii nagu lõpmata kõrgete seintega ristkülikukujulise potentsiaalikaevu elektroni puhul viivad piirtingimused konkreetsete võimalike ψ ja energia väärtusteni, nii vesinikuaatomile vastavas potentsiaalikaevus viivad füüsikalised tingimused võimalike väärtusteni. f1-st, f 2, f 3 ja seega ψ-funktsioonid. See ilmub ka siin peamine omadus kvantmehaanilised süsteemid – olekute diskreetsus.
Diskreetsus seisneb matemaatiliselt selles, et mis tahes võrrandi (28.23) funktsioonil on terve hulk (spekter) lahendusi, millest igaüks vastab teatud kvantarvule. Vastupidiselt ristkülikukujulisele lõpmatult kõrgete seintega potentsiaalikaevule iseloomustab elektroni olekut aatomis mitte üks, vaid mitu kvantarvu 1 . Esimene neist - peamine kvantarv P - 1, 2, 3... See määrab elektroni energiatasemed vastavalt seadusele:

See avaldis on Schrödingeri võrrandi lahendus ja ühtib täielikult Bohri teooria vastava valemiga (vt 28.7).
Joonisel fig. 28.11 näitab vesinikuaatomi koguenergia võimalike väärtuste tasemeid (E 1, E 2, E 3 jne) ja potentsiaalse energia E P sõltuvuse graafikut kaugusest. r elektroni ja tuuma vahel [vt (28.22)]. Peamise kvantarvu suurenedes P suureneb r[vt näiteks (28.33)] ja täielik [vt. (28.24)] ja potentsiaalne energia kipub nulli. Ka kineetiline energia kipub nulli minema. Varjutatud ala (E > 0) vastab vaba elektroni olekule.
1 Üldjuhul on kvantarvud täisarvud (0, 1, 2...) või pooltäisarvud (1/2, 3/2, 5/2...) arvud, mis määravad võimalikud diskreetsed väärtused füüsikalised kogused, mis iseloomustavad kvantsüsteeme ja elementaarosakesi.

1 Spinni olemasolu osakestes ei tulene Schrödingeri võrrandist.
selle arvutusega: rohkem aega oli see suurema tõenäosustihedusega kohtades, vähem pikk - väiksema tõenäosustihedusega kohtades. Filmile särituse tulemusena saadi erineva intensiivsusega kohad, mis illustreerivad elektroni jaotust aatomis. Joonistelt on näha, kui tinglik ja isegi ebaõige on mõiste “orbiit” elektroni liikumise suhtes.
Spin ja orbiidi magnetmomendid interakteeruvad üksteisega, mis muudab aatomi energiatasemete süsteemi võrreldes sellega, mis oleks ilma sellise vastastikmõjuta. Öeldakse, et spin-orbiidi interaktsioon viib peen struktuur energiatasemed. Kui see on märkimisväärne, siis on vaja arvestada elektroni kogu nurkimpulssiga - orbitaal pluss spin. Vahepeal selle asemel m l ja Prl kasutage muid kvantarve: j ja nij.
kvantarv j- orbitaal pluss spin - määrab kogu nurkimpulsi diskreetsed väärtused L elektron:

Magnetiline kvantarv m) iseloomustab kogu nurkimpulsi võimalikke projektsioone mõnele meelevaldselt valitud suunale Z:
Etteantud jaoks l kvantarv j võtab kaks väärtust: ±1/2
(Tabel 28.1).
Tabel 28.1

Etteantud jaoks j kvantarv nij võtab 2j + 1 väärtused: -j, -j + 1 ... + j.
28.7. BOORI TEOORIA MÕISTE
Taani füüsik N. Bohr pakkus juba enne kvantmehaanika loomist 1913. aastal välja vesinikuaatomi ja vesinikulaadsete ioonide teooria, mis põhines aatomi tuumamudelil ja selle kahel postulaadil. Bohri postulaadid ei mahtunud klassikalise füüsika raamidesse.
Esimese postulaadi kohaselt võivad aatom ja aatomisüsteemid pikka aega püsida ainult teatud statsionaarsetes olekutes. Sellistes olekutes aatom ei eralda ega neela energiat. Statsionaarsed olekud vastavad diskreetsetele energiaväärtustele: E 1, E 2...
Igasugune muutus aatomi või aatomisüsteemi energias on seotud järsu üleminekuga ühest paigalseisundist teise.
Teise postulaadi kohaselt kiirgab või neelab aatom aatomi üleminekul ühest olekust teise footoni, mille energia määratakse võrrandiga (29.1).
Üleminek kõrgema energiaga olekust madalama energiaga olekusse kaasneb footoni emissiooniga. Pöördprotsess on võimalik, kui footon neeldub.
Bohri teooria kohaselt tiirleb vesinikuaatomis olev elektron ringikujulisel orbiidil ümber tuuma. Kõigist võimalikest orbiitidest vastavad statsionaarsetele olekutele ainult need, mille nurkimpulss on täisarv h/(2π):
(n = 1, 2, 3...), (28,31)
kus m- elektroni mass; υ η - selle kiirus sisse lülitatud n-s orbiit; rn on selle raadius. Aatomis ringorbiidil pöörlevale elektronile mõjub positiivselt laetud tuuma küljelt lähtuv Coulombi tõmbejõud, mis Newtoni teise seaduse järgi võrdub elektroni massi ja tsentripetaalkiirenduse korrutisega (rekord on antud vaakumi jaoks):

Hoolimata Bohri teooria suurest edust ilmnesid peagi selle puudused. Seega ei olnud selle teooria raames võimalik seletada spektrijoonte intensiivsuse erinevust, s.o. vastake küsimusele, miks mõned energiasiirded on tõenäolisemad kui teised. Bohri teooria ei paljastanud keerukama aatomisüsteemi – heeliumiaatomi (kaks elektroni tiirlevad ümber tuuma) – spektraalmustreid.
Bohri teooria puuduseks oli selle ebaühtlus. See teooria ei olnud klassikaline ega kvant, see ühendas põhimõtteliselt erinevate teooriate sätted: klassikalise ja kvantfüüsika. Nii näiteks arvatakse Bohri teoorias, et elektron pöörleb aatomis teatud orbiidil (klassikalised esitused), kuid see ei kiirga elektromagnetlainet (kvantrepresentatsioonid).
Meie sajandi esimesel veerandil sai selgeks, et Bohri teooria tuleb asendada teise aatomiteooriaga. Ilmus kvantmehaanika.
28.8. KOMPLEKSSETE ATOMIDE ELEKTROONIKAKESTID
Kvantarvud, mis kirjeldavad elektroni olekut vesinikuaatomis, kasutatakse üksikute elektronide oleku ligikaudseks määramiseks kompleksaatomites. Siiski tuleks arvesse võtta vähemalt kahte olulist erinevust kompleksaatomite ja vesinikuaatomi vahel:
1) keerulistes aatomites ei sõltu elektronide energia nende vastasmõju tõttu mitte ainult n-st, vaid ka /-st;
2) erinevus tuleneb Pauli printsiibist, mille kohaselt aatomil ei saa olla kahte (või enamat) nelja identse kvantarvuga elektroni.
Normaalolekule vastava elektroonilise konfiguratsiooni moodustamisel kipub aatomi igal elektronil olema madalaim energia. Kui poleks Pauli põhimõtet, siis asuksid kõik elektronid madalaimal energiatasemel. Tegelikult hõivavad elektronid mõne erandiga olekute jada, mis on tabelis vesinikuaatomi jaoks näidatud. 29.
Sama peamise kvantarvuga elektronid moodustavad kihi. Kihid on nn TO, L M, N jne. kooskõlas n= 1, 2, 3, 4... Elektronid, millel on sama väärtusega paarid n ja / , on osa kestast, mida lühidalt tähistatakse samamoodi nagu vesinikuaatomi elektroni vastavaid olekuid: 1s, 2s, 2^ jne. Nii nimetatakse näiteks 2s kest, 2s elektronid jne.
Elektronide arv kestas on näidatud üleval paremal kesta sümboolse tähise lähedal, näiteks 2p 4 .
Elektronide jaotus aatomi kestade vahel (elektroonilised konfiguratsioonid) on tavaliselt näidatud järgmiselt: lämmastiku puhul 1s 2, 2s2, 2p 3, kaltsiumi jaoks 1s 2, 2s 2, 2p 6, 3s 2, 3p 6, 4s 2 jne.
Kuna keeruliste aatomite elektronide energia ei sõltu mitte ainult n-st, vaid ka l, siis perioodilisustabeli konstrueerimine ei toimu alati kihtide järkjärgulise täitmisega, kuna aatom muutub keerukamaks. Kaaliumi jaoks (Z = 19) näiteks kihi täitmise asemel M(see võis olla 1s 2, 2s 2, 2^ 6, 3s 2, 3p 6, 3a 1) algab kihi täitmine N ja looge järgmine elektrooniline konfiguratsioon: 1 s2, 2s 2, 2p 6, 3s 2, 3p 6, 4s 1.
Ka teistel elementidel on tavapärasest kihtide täitmisest sarnased kõrvalekalded.
Alati jooksmas üldreegel: ergastamata aatomi elektronid hõivavad madalaima energiaga oleku ja järgivad Pauli printsiipi. Joonisel fig. 28.13 on skemaatiliselt, skaalat arvestamata, näidatud kompleksse aatomi energiaseisundid ja vastav elektronide arv.
Kokkuvõtteks märgime, et mitmeelektronilise aatomi oleku kui terviku määravad järgmised kvantarvud: L- aatomi kogu orbitaalmoment, mis võtab väärtused 0, 1, 2, 3 jne. üks ; J- aatomi summaarne moment, mis võib võtta väärtusi intervalliga üks alates |L - S| kuni |L + S |; S- tekkiv aatomi pöörlemismoment; magnetiline m J , mis määrab aatomi koguimpulsi projektsiooni diskreetsed väärtused mõnele teljele Z:

Etteantud jaoks Jm J võtab 2 J+ 1 väärtused:
-J, -J+ 1 ... +J.
1 Ärge ajage seda nimetust elektroonilise kihi nimega segamini L ja elektroni kogu nurkimpulssiga.
28.9. Molekulide energiatase
Kuna molekulid koosnevad aatomitest, on molekulisisene liikumine keerulisem kui aatomisisene liikumine. Molekulis on lisaks elektronide liikumisele tuumade suhtes võnkuv liikumine aatomid oma tasakaaluasendi ümber (tuumade vibratsioon koos neid ümbritsevate elektronidega) ja molekuli kui terviku pöörlev liikumine.
Elektrooniline, võnkuv ja pöörlevad liigutused molekulid vastavad kolme tüüpi energiatasemetele: E el, E count ja E time. Kvantmehaanika järgi võtab igat tüüpi liikumise energia molekulis ainult diskreetseid väärtusi (kvanteeritud). Esitagem ligikaudu molekuli koguenergiat E erinevat tüüpi energiate kvantiseeritud väärtuste summana:
E\u003d E el + E arv + E aeg. (28.37)
Joonisel fig. 28.14 kujutab skemaatiliselt molekuli tasemesüsteemi: kaugel asetsevad elektroonilised energiatasemed a" ja a"", mille puhul E count = E vr = 0; tihedamalt asetsevad vibratsioonitasemed v" , v"", nende jaoks E r = 0; kõige tihedamini asetsevad pöörlemistasemed J" ja J"" erinevate E aja väärtustega.
Vahemaa elektroonilised tasemed energiad suurusjärgus mitu elektronvolti, külgnevate võnketasemete vahel 10 -2 -10 -1 eV, külgnevate pöörlemistasemete vahel 10 -5 -10 -3 eV.

Valgusel on nii laine- kui ka osakeste omadused. Laine omadused ilmnevad valguse levimise ajal (häired, difraktsioon). Korpuskulaarsed omadused avalduvad valguse vastasmõjus ainega (fotoelektriline efekt, valguse emissioon ja neeldumine aatomite poolt).
Footoni kui osakese omadused (energia E ja impulss p) on seotud tema laineomadustega (sagedus ν ja lainepikkus λ) seostega.
; , (19)
kus h = 6,63 × 10 -34 J - Plancki konstant.
Püüdes ületada Bohri aatomimudeli raskusi, esitas prantsuse füüsik Louis de Broglie 1924. aastal hüpoteesi, et laine ja korpuskulaarsete omaduste kombinatsioon on omane mitte ainult valgusele, vaid ka igale materiaalsele kehale. See tähendab, et aineosakestel (näiteks elektronidel) on lainelised omadused. de Broglie sõnul vastab iga keha massiga m, mis liigub kiirusega υ, laineprotsessile lainepikkusega.
Kõige ilmekamad laineomadused avalduvad mikroobjektides (elementaarosakestes). Väikese massi tõttu osutub de Broglie lainepikkus võrreldavaks kristallide aatomitevahelise kaugusega. Nendes tingimustes põhjustab osakeste kiire interaktsioon kristallvõrega difraktsiooninähtusi. Elektronid energiaga 150 eV vastab lainepikkusele λ»10 -10 m. Aatomitevahelised kaugused kristallides on samas järjekorras. Kui selliste elektronide kiir suunatakse kristallile, siis need hajuvad difraktsiooniseaduste kohaselt. Fotofilmile salvestatud difraktsioonimuster (elektronide difraktsioonimuster) sisaldab teavet kolmemõõtmelise struktuuri kohta. kristallvõre.

Joonis 6 Aine laineomaduste illustratsioon
Osakeste laineomaduste illustreerimiseks kasutatakse sageli mõtteeksperimenti – elektronkiire (või muude osakeste) läbimist läbi Δx laiuse pilu. Vaatenurgast uus teooria pärast pilu poolt difraktsiooni laieneb kiir nurkdivergentsiga θ»λ/Δх. Korpuskulaarsest vaatepunktist on kiire laienemine pärast pilu läbimist seletatav teatud põikimpulsi ilmnemisega osakestes. Selle põikimpulsi ("määramatus") väärtuste levik on
![]() (21)
(21)
Suhe (22)
nimetatakse määramatuse suhteks. See suhe korpuskulaarses keeles peegeldab osakeste laineomaduste olemasolu.
Katse elektronkiire läbimise kohta läbi kahe tihedalt asetseva pilu võib olla veelgi selgem näide osakeste laineomadustest. See katse on analoogne Youngi optiliste häirete katsega.
4. 10 Aatomi kvantmudel Eksperimentaalsed faktid (elektronide difraktsioon, Comptoni efekt, fotoelektriline efekt ja paljud teised) ja teoreetilised mudelid, nagu Bohri aatomimudel, näitavad selgelt, et klassikalise füüsika seadused muutuvad aatomite ja molekulide käitumise kirjeldamisel kohaldamatuks. nende koostoime valgusega. Aastakümnel 1920–1930 mitmed kahekümnenda sajandi silmapaistvad füüsikud. (de Broglie, Heisenberg, Born, Schrödinger, Bohr, Pauli jt) tegeles teooria konstrueerimisega, mis suudab adekvaatselt kirjeldada mikromaailma nähtusi. Selle tulemusena sündis kvantmehaanika, millest sai kõigi kaasaegsete aine struktuuri teooriate alus, võib öelda, et kahekümnenda sajandi füüsika alus (koos relatiivsusteooriaga).
Mikrokosmoses kehtivad kvantmehaanika seadused, samas oleme makroskoopilised objektid ja elame makrokosmoses, mida juhivad hoopis teised, klassikalised seadused. Seetõttu pole üllatav, et paljusid kvantmehaanika sätteid ei saa me otse kontrollida ja neid tajutakse kummaliste, võimatute, ebatavalistena. Sellegipoolest on kvantmehaanika tõenäoliselt eksperimentaalselt kõige enam kinnitatud teooria, kuna selle teooria seaduste järgi tehtud arvutuste tagajärgi kasutatakse peaaegu kõiges, mis meid ümbritseb ja on saanud osaks inimtsivilisatsioonist (piisab, kui mainida neid pooljuhtelemente, tööd mis praegu võimaldavad lugejal näha monitori ekraanil teksti, mille katvus, muide, on samuti arvutatud kvantmehaanika abil).
Kahjuks on kvantmehaanika kasutatav matemaatiline aparaat üsna keeruline ja kvantmehaanika ideid saab välja öelda vaid verbaalselt ja seetõttu mitte piisavalt veenvalt. Seda märkust silmas pidades püüame anda nendest ideedest vähemalt mingi ettekujutuse.
Kvantmehaanika põhimõiste on mingi mikroobjekti ehk mikrosüsteemi kvantseisundi mõiste (see võib olla üksik osake, aatom, molekul, aatomite kogum jne).
Aatomi kvantmudel erineb planetaarsest esiteks selle poolest, et selles sisalduval elektronil ei ole täpselt määratletud koordinaati ja kiirust, mistõttu pole mõtet rääkida tema liikumise trajektoorist. On võimalik määrata (ja joonistada) ainult selle valdava liikumise piirkonna (orbitaalide) piire.
Mõne mikroobjekti või mikrosüsteemi (see võib olla eraldi osake, aatom, molekul, aatomite kogum jne) olekut saab iseloomustada kvantarvude seadmisega: energia, impulsi, impulsi momendi väärtused, selle tõukemomendi projektsioon mõnele teljele, laengule jne.
SCHROEDINGERI VÕRD elektroni liikumise jaoks vesinikuaatomi tuuma Coulombi väljas kasutatakse aatomi kvantmudeli analüüsimiseks. Selle võrrandi lahendamise tulemusena saadakse lainefunktsioon, mis ei sõltu ainult koordinaadist ja ajast t, vaid ka 4 parameetrist, millel on diskreetne väärtuste kogum ja mida nimetatakse kvantarvudeks. Neil on nimed: põhi-, asimuut-, magnet- ja magnetspinn.
Peamine kvantarv n võib võtta täisarvu väärtused 1, 2, ... . See määrab elektroni energia aatomis
Kus E i on vesinikuaatomi ionisatsioonienergia (13,6 eV).
ASIMUTAALNE (ORBITAALNE) kvantarv l
määrab elektroni nurkimpulsi mooduli tema orbitaalliikumise ajal ![]() (24)
kus s on spinn-kvantarv, millel on iga osakese jaoks ainult üks väärtus. Näiteks elektroni puhul s = (sarnaselt prootoni ja neutroni puhul). Footoni puhul s = 1.
(24)
kus s on spinn-kvantarv, millel on iga osakese jaoks ainult üks väärtus. Näiteks elektroni puhul s = (sarnaselt prootoni ja neutroni puhul). Footoni puhul s = 1.
Degenereerunud nimetatakse sama energiaga elektroni olekuid.
MITMELINE DEGENERATSIOON on võrdne sama energiaga olekute arvuga.
LÜHIÜHEND elektroni oleku registreerimine aatomis: NUMBER, võrdne peamise kvantarvuga ja tähega, mis määrab asimuutkvantarvu:
Tabel 1 Lühiülevaade elektroni oleku kohta aatomis
Muidugi võib seda jaburaks nimetada,
aga olen kohanud sellist jama, et sisse
temaga võrreldes tundub see mõistlik
sõnastik.
L. Carroll
Mis on juhtunud planetaarne mudel aatom ja mis on selle puudused? Mis on Bohri aatomimudeli olemus? Mis on hüpotees osakeste laineomaduste kohta? Milliseid ennustusi see hüpotees mikromaailma omaduste kohta annab?
Tund-loeng
Aatomi KLASSIKALISED MUDELID JA NENDE MIINUSED. Ideed, et aatomid ei ole jagamatud osakesed ja sisaldavad osakestena elementaarlaenguid, väljendati esmakordselt XIX lõpus v. Termini "elektron" pakkus 1881. aastal välja inglise füüsik George Stoney. 1897. aastal sai elektronhüpotees eksperimentaalne kinnitus Emil Wiecherti ja Joseph John Thomsoni õpingutes. Sellest hetkest algas erinevate aatomite ja molekulide elektrooniliste mudelite loomine.
Thomsoni esimene mudel eeldas, et positiivne laeng on aatomis ühtlaselt jaotunud ja elektronid olid sellesse pikitud nagu rosinad kukli sees.
Selle mudeli ja katseandmete lahknevus selgus pärast 1906. aastal Ernest Rutherfordi katset, kes uuris α-osakeste hajumise protsessi aatomite kaudu. Kogemusest järeldati, et positiivne laeng on koondunud moodustise sisse, palju väiksem kui aatomi suurus. Seda moodustist nimetatakse aatomituum, mille mõõtmed olid 10 -12 cm ja aatomi mõõtmed - 10 -8 cm Vastavalt elektromagnetismi klassikalistele ideedele peab iga elektroni ja tuuma vahel toimima Coulombi tõmbejõud. Selle jõu sõltuvus kaugusest peaks olema sama, mis seaduses gravitatsiooni. Seetõttu peab elektronide liikumine aatomis olema sarnane planeetide liikumisega. Päikesesüsteem. Nii sündis aatomi planetaarmudel Rutherford.
Aatomi lühike eluiga ja pidev kiirgusspekter, mis tulenevad planeedimudelist, näitasid selle ebajärjekindlust elektronide liikumise kirjeldamisel aatomis.
Edasine aatomi stabiilsuse uuring andis vapustava tulemuse: arvutused näitasid, et 10 -9 s jooksul peab elektron kiirguse energiakao tõttu tuumale langema. Lisaks andis selline mudel aatomite pidevad, mitte diskreetsed emissioonispektrid.
BOORIAatomi TEOORIA. Järgmise olulise sammu aatomiteooria arendamisel tegi Niels Bohr. Kõige olulisem hüpotees, mille Bohr esitas 1913. aastal, oli hüpotees elektroni energiatasemete diskreetsest struktuurist aatomis. Seda asendit illustreerivad energiadiagrammid (joonis 21). Traditsiooniliselt kujutavad energiadiagrammid energiat piki vertikaaltelge.
Riis. 21 Satelliidi energia Maa gravitatsiooniväljas (а); elektroni energia aatomis (b)
Keha liikumise erinevus gravitatsiooniväljas (joonis 21, a) ja elektroni liikumise vahel aatomis (joonis 21, b) Bohri hüpoteesi kohaselt seisneb selles, et keha energia võib pidevalt muutuda ja negatiivsete väärtustega elektroni energia võib võtta joonisel näidatud seeria diskreetseid väärtusi siniste segmentidena. Neid diskreetseid väärtusi nimetati energiatasemeteks või teisisõnu energiatasemeteks.
Muidugi, idee diskreetsetest energiatasemetest võeti Plancki hüpoteesist. Elektroni energia muutus sai Bohri teooria kohaselt toimuda ainult hüppel (ühelt energiatasemelt teisele). Nende üleminekute ajal kiirgab (üleminek alla) või neeldub valguskvant (üleminek), mille sagedus määratakse aatomi Plancki valemiga hv \u003d E kvant \u003d ΔE, st aatomi energia muutus. aatom on võrdeline kiiratava või neeldunud valguskvanti sagedusega.
Bohri teooria selgitas suurepäraselt aatomispektrite joonte iseloomu. Küsimusele tasandite diskreetsuse põhjuse kohta teooria aga tegelikult vastust ei andnud.
AINE LAINED. Järgmise sammu mikromaailma teooria arendamisel tegi Louis de Broglie. 1924. aastal pakkus ta välja, et mikroosakeste liikumist tuleks kirjeldada mitte klassikalise mehaanilise liikumisena, vaid mingisuguse laineliikumisena. Just laineliikumise seadustest tulebki saada retseptid erinevate vaadeldavate suuruste arvutamiseks. Nii et teaduses koos lainetega elektromagnetväli tekkisid ainelained.
Hüpotees osakeste liikumise lainelise olemuse kohta oli sama julge kui Plancki hüpotees välja diskreetsete omaduste kohta. Katse, mis kinnitas otseselt de Broglie hüpoteesi, püstitati alles aastal 1927. Selles katses täheldati elektronide difraktsiooni kristallil, mis sarnaneb elektromagnetlaine difraktsiooniga.
Bohri teooria oli oluline samm mikromaailma seaduste mõistmisel. See oli esimene, kes tutvustas aatomis oleva elektroni energia diskreetsete väärtuste sätet, mis vastas kogemusele ja sai hiljem kvantteooria osaks.
Aine lainete hüpotees võimaldas selgitada energiatasemete diskreetsust. Laineteooriast oli teada, et ruumis piiratud lainel on alati diskreetsed sagedused. Näiteks on laine sellises muusikainstrument nagu flööt. Helisageduse määravad sel juhul ruumi mõõtmed, millega laine on piiratud (flöödi mõõtmed). Selgub, et see on lainete üldine omadus.
Kuid Plancki hüpoteesi kohaselt on elektromagnetlaine kvantide sagedused võrdelised kvanti energiaga. Järelikult peab ka elektronide energia võtma diskreetseid väärtusi.
De Broglie idee osutus väga viljakaks, kuigi, nagu juba mainitud, viidi otsene elektroni laineomadusi kinnitav katse läbi alles 1927. aastal. vesinikuaatom sai kõik tulemused, milleks Bohri teooria oli võimeline. andes. Tegelikult sai sellest alguse kaasaegne teooria, mis kirjeldas mikrokosmoses toimuvaid protsesse, kuna lainevõrrand oli enamiku jaoks kergesti üldistatav. erinevad süsteemid- mitmeelektronilised aatomid, molekulid, kristallid.
Teooria areng viis arusaamisele, et osakesele vastav laine määrab ära tõenäosuse osakest antud ruumipunktis leida. Nii sisenes tõenäosuse mõiste mikrokosmose füüsikasse
Uue teooria järgi määrab osakesele vastav laine täielikult osakese liikumise. Aga üldised omadused lained on sellised, et lainet ei saa lokaliseerida üheski ruumipunktis, st osakese koordinaatidest antud ajahetkel rääkida on mõttetu. Selle tagajärjeks oli selliste mõistete nagu osakese trajektoor ja elektronide orbiidid aatomis täielik väljajätmine mikrokosmose füüsikast. Ilus ja visuaalne aatomi planetaarmudel, nagu selgus, ei vasta elektronide tegelikule liikumisele.
Kõik protsessid mikrokosmoses on tõenäosuslikud. Arvutustega saab määrata ainult konkreetse protsessi toimumise tõenäosust.
Lõpetuseks pöördume tagasi epigraafi juurde. Hüpoteesid mateerialainete ja väljakvantide kohta tundusid paljudele füüsikutele, kes olid üles kasvanud klassikalise füüsika traditsioonide järgi, jaburana. Fakt on see, et need hüpoteesid jäävad ilma tavalisest visualiseerimisest, mis meil on makrokosmoses vaatlusi tehes. Mikromaailma teaduse hilisem areng viis aga selliste ideedeni, mis ... (vt lõigu epigraafi).
- Milliste eksperimentaalsete faktidega Thomsoni aatomimudel vastuolus oli?
- Mis on Bohri aatomimudelist tänapäeva teoorias alles jäänud ja mis on kõrvale jäetud?
- Millised ideed aitasid kaasa de Broglie hüpoteesile aine lainete kohta?
Bohri teooria puudujäägid viitasid vajadusele vaadata üle kvantteooria alused ja ideed mikroosakeste olemusest (elektronid, prootonid jne). Tekkis küsimus, kui terviklik on elektroni kujutamine väikese mehaanilise osakese kujul, mida iseloomustavad kindlad koordinaadid ja teatud kiirus.
Teame juba, et optilistes nähtustes on täheldatav omamoodi dualism. Koos difraktsiooni-, interferentsi- (lainenähtustega) täheldatakse ka valguse korpuskulaarsust iseloomustavaid nähtusi (fotoelektriline efekt, Comptoni efekt).
1924. aastal püstitas Louis de Broglie selle hüpoteesi dualism ei ole ainult optiliste nähtuste tunnus ,kuid on universaalne. Aineosakestel on ka lainelised omadused .
"Optikas," kirjutas Louis de Broglie, "sajand oli korpuskulaarne kaalutlusmeetod lainega võrreldes liiga tähelepanuta jäetud; Kas aineteoorias on tehtud vastupidine viga? Eeldusel, et aineosakestel on koos korpuskulaarsete omadustega ka lainelised omadused, kandis de Broglie aineosakeste puhul üle samad ühelt pildilt teisele ülemineku reeglid, mis kehtivad valguse puhul.
Kui footonil on energia ja impulss, siis teatud kiirusega liikuval osakesel (näiteks elektronil) on lainelised omadused, s.t. osakeste liikumist võib pidada laineliseks liikumiseks.
Kvantmehaanika järgi osakese vaba liikumine massiga m ja impulsi (kus υ on osakese kiirus) saab esitada tasapinnalise monokromaatilise lainena ( de Broglie laine) lainepikkusega
| (3.1.1) |
levib samas suunas (näiteks telje suunas X), milles osake liigub (joonis 3.1).

Lainefunktsiooni sõltuvus koordinaadist X on antud valemiga
| , | (3.1.2) |
kus - laine number ,a laine vektor suunatud laine levimise suunas või piki osakese liikumist:
| . | (3.1.3) |
Sellel viisil, monokromaatilise laine lainevektor seotud vabalt liikuva mikroosakesega, võrdeline selle impulsiga või pöördvõrdeline selle lainepikkusega.
Kuna suhteliselt aeglaselt liikuva osakese kineetiline energia , siis saab lainepikkust väljendada ka energiana:
| . | (3.1.4) |
Kui osake interakteerub mõne objektiga – kristalli, molekuli vms. – selle energia muutub: sellele lisandub selle vastasmõju potentsiaalne energia, mis toob kaasa muutuse osakese liikumises. Sellest lähtuvalt muutub osakesega seotud laine levimise iseloom ja see toimub vastavalt kõikidele lainenähtustele ühistele põhimõtetele. Seetõttu ei erine osakeste difraktsiooni põhilised geomeetrilised seaduspärasused mitte millegi poolest ühegi lainete difraktsiooni seaduspärasustest. Mis tahes laadi lainete difraktsiooni üldtingimuseks on langeva lainepikkuse võrreldavus λ distantsiga d hajumiskeskuste vahel: .
Louis de Broglie hüpotees oli revolutsiooniline isegi selle murrangulise aja jooksul teaduses. Kuid peagi kinnitasid seda paljud katsed.
20. sajandi alguseks olid optikas tuntud nii nähtused, mis kinnitasid laineomaduste olemasolu valguses (interferents, polarisatsioon, difraktsioon jne), kui ka korpuskulaarteooria seisukohalt seletatud nähtusi (fotoelektriline efekt, Compton). mõju jne). 20. sajandi alguses avastati aineosakestele mitmeid lainetele iseloomulike optiliste nähtustega väliselt sarnaseid mõjusid. Nii leidis Ramsauer 1921. aastal argooni aatomitel elektronide hajumist uurides, et kui elektronide energia väheneb mitmekümne elektronvoldi võrra, suureneb argoonil elektronide elastse hajumise efektiivne ristlõige (joonis 4.1).
Kuid elektronenergial ~16 eV saavutab efektiivne ristlõige maksimumi ja väheneb elektronenergia edasise vähenemisega. Elektroni energial ~ 1 eV muutub see nullilähedaseks ja hakkab seejärel uuesti kasvama.
Seega ei paista elektronid ~ 1 eV lähedal kokkupõrkeid argooni aatomitega ja lendavad läbi gaasi ilma hajumiseta. Sama käitumine on iseloomulik ka elektronide hajumise ristlõikele inertgaaside teiste aatomite, aga ka molekulide poolt (viimase avastas Townsend). See efekt on analoogne Poissoni laigu tekkega valguse difraktsiooni käigus väikesel ekraanil.
Veel üks huvitav efekt on elektronide selektiivne peegeldumine metallide pinnalt; seda uurisid 1927. aastal Ameerika füüsikud Davisson ja Germer ning ka iseseisvalt inglise füüsik J. P. Thomson.
Katoodkiiretorust (joonis 4.2) tulev paralleelne monoenergeetiliste elektronide kiir suunati nikkelplaadile. Peegeldunud elektronid püüdis kinni galvanomeetriga ühendatud kollektor. Kollektor paigaldatakse langeva tala suhtes mis tahes nurga all (kuid sellega samas tasapinnas).
Davisson-Jermeri katsete tulemusena selgus, et hajutatud elektronide nurkjaotus on sama iseloomuga kui kristalli hajutatud röntgenikiirguse jaotus (joonis 4.3). Uurides röntgenkiirte difraktsiooni kristallidel, leiti, et difraktsioonimaksimumide jaotust kirjeldatakse valemiga
kus on võre konstant, on difraktsiooni järjekord, on röntgenikiirguse lainepikkus.
Raske tuuma poolt neutronite hajumise korral tekkis ka hajutatud neutronite tüüpiline difraktsioonijaotus, mis on sarnane optika puhul täheldatule, kui valgust hajutab neelduv ketas või kuul.
Prantsuse teadlane Louis de Broglie väljendas 1924. aastal ideed, et aineosakestel on nii korpuskulaarsed kui ka lainelised omadused. Samal ajal pakkus ta välja, et konstantse kiirusega vabalt liikuv osake vastab tasapinnalisele monokromaatilisele lainele
kus ja on selle sagedus ja lainevektor.
Laine (4.2) levib osakese () liikumissuunas. Selliseid laineid nimetatakse faasilained, aine lained või de Broglie lained.
De Broglie idee oli laiendada analoogiat optika ja mehaanika vahel ning võrrelda laineoptikat lainemehaanikaga, püüdes viimast rakendada aatomisiseste nähtuste puhul. Katse omistada elektronile ja üldiselt kõigile osakestele, nagu footonid, kahetine olemus, andes neile lainelised ja korpuskulaarsed omadused, mis on omavahel seotud tegevuskvantiga – selline ülesanne tundus äärmiselt vajalik ja viljakas. "... On vaja luua uus lainelise iseloomuga mehaanika, mis seostuks vana mehaanikaga nagu laineoptika geomeetrilise optikaga," kirjutas de Broglie oma raamatus "Revolution in Physics".
Kiirusega liikuval massiosakel on energia
ja hoogu
ja osakeste liikumise olekut iseloomustab neljamõõtmeline energia-impulsi vektor ().
Teisest küljest kasutame lainemustris sageduse ja lainearvu (või lainepikkuse) mõistet ning tasapinnalisele lainele vastav 4-vektor on ().
Kuna mõlemad ülaltoodud kirjeldused on sama füüsilise objekti erinevad aspektid, peab nende vahel olema ühemõtteline seos; relativistlikult invariantne seos 4-vektori vahel on
Avaldised (4.6) kutsutakse de Broglie valemid. De Broglie lainepikkus määratakse seega valemiga
(siin). Just see lainepikkus peaks kajastuma Ramsauer-Townsendi efekti lainekirjelduse ja Davissoni-Jermeri katsete valemites.
Elektronide jaoks kiirendatud elektriväli potentsiaalide erinevusega B, de Broglie lainepikkus nm; kV juures = 0,0122 nm. Vesiniku molekuli puhul, mille energia J (temperatuuril = 300 K) = 0,1 nm, mis langeb suurusjärgus kokku röntgenikiirte lainepikkusega.
Võttes arvesse (4.6), saab valemi (4.2) kirjutada tasapinnaliseks laineks
vastav osake impulsi ja energiaga.
De Broglie laineid iseloomustavad faasi- ja rühmakiirused. Faasi kiirus määratakse laine faasi püsivuse tingimusest (4.8) ja relativistliku osakese jaoks on võrdne
see tähendab, et see on alati suurem kui valguse kiirus. rühma kiirus de Broglie lained on võrdne osakese kiirusega:
(4.9) ja (4.10) põhjal on de Broglie lainete faasi- ja grupikiiruste vaheline seos järgmine:
Mis on füüsiline tähendus de Broglie lained ja milline on nende suhe aineosakestega?
Osakese liikumise lainekirjelduse raames tõi olulise epistemoloogilise keerukuse esile tema ruumilise lokaliseerimise küsimus. De Broglie lained (4.2), (4.8) täidavad kogu ruumi ja eksisteerivad piiramatult. Nende lainete omadused on alati ja kõikjal ühesugused: nende amplituud ja sagedus on konstantsed, lainepindade vahelised kaugused on muutumatud jne. Teisest küljest säilitavad mikroosakesed oma korpuskulaarsed omadused, st neil on teatud mass lokaliseeritud teatud ruumipiirkonnas. Sellest olukorrast väljumiseks hakati osakesi esindama mitte monokromaatsed de Broglie lained, vaid lähedase sagedusega lainete komplektid (lainenumbrid) - lainepaketid:

sel juhul on amplituudid nullist erinevad ainult lainete puhul, mille lainevektorid sisalduvad intervallis (). Kuna lainepaketi grupikiirus on võrdne osakese kiirusega, tehti ettepanek esitada osakest lainepaketi kujul. Kuid see idee on vastuvõetamatu järgmistel põhjustel. Osake on stabiilne moodustis ega muutu oma liikumise ajal sellisena. Lainepaketil, mis väidetavalt esindab osakest, peavad olema samad omadused. Seetõttu on vaja nõuda, et lainepakett säilitaks aja jooksul oma ruumilise kuju või vähemalt laiuse. Kuna aga faasikiirus oleneb osakese impulsist, siis (isegi vaakumis!) peab olema de Broglie lainete dispersioon. Selle tulemusena rikutakse paketi lainete vahelisi faasisuhteid ja pakett levib. Seetõttu peab sellise paketiga esindatud osake olema ebastabiilne. See järeldus on vastuolus kogemusega.
Lisaks esitati vastupidine oletus: osakesed on primaarsed ja lained esindavad nende moodustisi, see tähendab, et need tekivad nagu heli osakestest koosnevas keskkonnas. Kuid selline keskkond peab olema piisavalt tihe, sest osakeste keskkonnas on lainetest mõtet rääkida alles siis, kui osakeste keskmine kaugus on lainepikkusega võrreldes väga väike. Ja katsetes, milles leitakse mikroosakeste laineomadusi, seda ei tehta. Kuid isegi kui see raskus ületatakse, tuleb näidatud seisukoht siiski tagasi lükata. Tõepoolest, see tähendab, et laineomadused on omane paljude osakeste süsteemidele, mitte üksikutele osakestele. Samal ajal ei kao osakeste lainelised omadused isegi langevate kiirte madala intensiivsuse korral. Bibermani, Sushkini ja Fabrikanti 1949. aastal läbi viidud katsetes kasutati nii nõrku elektronkiire, et keskmine ajavahemik kahe järjestikuse elektroni difraktsioonisüsteemi (kristalli) läbimise vahel oli 30 000 (!) korda pikem kui aeg. kulutab üks elektron kogu seadme läbimiseks. Sellistes tingimustes ei mänginud elektronide omavaheline interaktsioon loomulikult mingit rolli. Sellegipoolest tekkis piisavalt pika särituse korral kristalli taha asetatud fotofilmile difraktsioonimuster, mis ei erinenud millegi poolest elektronkiirte lühikese säritusega saadud mustrist, mille intensiivsus oli 10 7 korda suurem. Oluline on ainult see, et mõlemal juhul koguarv fotoplaati tabanud elektronid olid samad. See näitab, et üksikutel osakestel on ka lainelised omadused. Katse näitab, et üks osake ei anna difraktsioonimustrit, iga üksiku elektron põhjustab fotoplaadi mustaks muutumist väikesel alal. Kogu difraktsioonimustri saab saada ainult plaati löödes suur hulk osakesed.
Vaatlusaluses katses olev elektron säilitab täielikult oma terviklikkuse (laeng, mass ja muud omadused). See näitab selle korpuskulaarseid omadusi. Samal ajal on ilmne ka laineomaduste avaldumine. Elektron ei taba kunagi fotoplaadi seda osa, kus difraktsioonimuster peaks olema minimaalne. See võib ilmuda ainult difraktsioonimaksimumide asukoha lähedal. Sel juhul on võimatu ette kindlaks määrata, millises konkreetses suunas antud osake lendab.
Mõte, et nii korpuskulaarsed kui ka lainelised omadused avalduvad mikroobjektide käitumises, on sätestatud mõistes. "osakeste-laine dualism" ja on kvantteooria aluseks, kus ta sai loomuliku tõlgenduse.
Born pakkus välja kirjeldatud katsete tulemuste nüüdseks üldtunnustatud tõlgenduse: tõenäosus, et elektron tabab fotoplaadi teatud punkti, on võrdeline vastava de Broglie laine intensiivsusega ehk laine ruuduga. välja amplituud teatud kohas ekraanil. Seega tehakse ettepanek tõenäosuslik-statistiline tõlgendus mikroosakestega seotud lainete olemus: mikroosakeste jaotumise regulaarsust ruumis saab kindlaks teha ainult suure hulga osakeste puhul; ühe osakese puhul saab määrata ainult teatud ala tabamise tõenäosust.
Pärast osakeste korpuskulaar-laine dualismiga tutvumist on selge, et klassikalises füüsikas kasutatavad meetodid ei sobi mikroosakeste mehaanilise oleku kirjeldamiseks. Kvantmehaanikas tuleb oleku kirjeldamiseks kasutada uusi spetsiifilisi vahendeid. Neist kõige olulisem on mõiste lainefunktsioon või olekufunktsioon (-funktsioonid).
Riigi funktsioon on matemaatiline pilt laineväljast, mis peaks olema seotud iga osakesega. Seega on vaba osakese olekufunktsiooniks tasapinnaline monokromaatiline de Broglie laine (4.2) või (4.8). Välismõjule allutatud osakese puhul (näiteks elektroni puhul tuumaväljas) võib sellel laineväljal olla väga keeruline vorm ja see muutub ajas. Lainefunktsioon sõltub mikroosakese parameetritest ja füüsikalistest tingimustest, milles osake asub.
Lisaks näeme seda kõige rohkem lainefunktsiooni kaudu Täielik kirjeldus mikroobjekti mehaaniline seisund, mis on võimalik ainult mikromaailmas. Teades lainefunktsiooni, on võimalik ennustada, milliseid kõigi mõõdetud suuruste väärtusi saab katseliselt jälgida ja millise tõenäosusega. Olekufunktsioon kannab kogu teavet osakeste liikumise ja kvantomaduste kohta, seetõttu räägitakse selle abil kvantoleku seadmisest.
Vastavalt de Broglie lainete statistilisele tõlgendusele määrab osakeste lokaliseerumise tõenäosuse de Broglie laine intensiivsus, nii et tõenäosus tuvastada osakest väikeses mahus punkti läheduses korraga on
Võttes arvesse funktsiooni keerukust, on meil:
Plaani de Broglie laine jaoks (4.2)
see tähendab, et sama suure tõenäosusega leiab ta vaba osakese kõikjalt ruumist.
väärtust
helistas tõenäosustihedus. Osakese leidmise tõenäosus korraga lõplikus mahus on tõenäosuse liitmise teoreemi kohaselt võrdne
Kui integreerida (4.16) lõpmatutes piirides, saame täieliku tõenäosusega osakese tuvastamine mingil ajahetkel kuskil ruumis. See on teatud sündmuse tõenäosus, nii et
Nimetatakse tingimus (4.17). normaliseerimisseisund, ja - funktsioon, mis seda rahuldab, - normaliseeritud.
Rõhutame veel kord, et jõuväljas liikuva osakese jaoks on funktsioon rohkem kompleksne tüüp kui de Broglie tasapinna laine (4.2).
Kuna funktsioon - on keeruline, saab seda esitada kui
kus on -funktsiooni moodul ja faasitegur, milles on mis tahes reaalarv. Selle avaldise ja (4.13) ühisest vaatlemisest on selge, et normaliseeritud lainefunktsioon on defineeritud mitmetähenduslikult, kuid ainult konstantse tegurini. Märgitud ebaselgus on põhiline ja seda ei saa kõrvaldada; see on siiski ebaoluline, kuna see ei mõjuta füüsilisi tulemusi. Tõepoolest, funktsiooni korrutamine eksponendiga muudab kompleksfunktsiooni faasi, kuid mitte selle moodulit, mis määrab tõenäosuse saada katses füüsikalise suuruse üks või teine väärtus.
Potentsiaaliväljas liikuva osakese lainefunktsiooni saab esitada lainepaketiga. Kui osakese liikumisel mööda telge on lainepaketi pikkus võrdne, siis ei saa selle tekkeks vajalikud lainearvud hõivata suvaliselt kitsast intervalli. Minimaalne intervalli laius peab rahuldama seost või pärast korrutamist
Sarnased seosed kehtivad piki telgede levivate lainepakettide puhul ja:
Seosed (4.18), (4.19) kutsutakse Heisenbergi määramatuse suhted(või määramatuse põhimõte). Selle kvantteooria põhiseisukoha kohaselt ei saa ükski füüsiline süsteem olla olekutes, kus selle inertskeskme ja impulsi koordinaadid võtavad samaaegselt üsna kindlaid, täpseid väärtusi.
Ülekirjutatutega sarnased seosed peavad kehtima iga niinimetatud kanooniliselt konjugeeritud suuruste paari puhul. Määramatuse suhetes sisalduv Plancki konstant seab piiri selliste suuruste samaaegse mõõtmise täpsusele. Samas on mõõtemääramatus seotud mitte katsetehnika ebatäiuslikkusega, vaid aineosakeste objektiivsete (laine)omadustega.
Teine oluline punkt mikroosakeste olekute arvestamisel on seadme mõju mikroobjektile. Iga mõõtmisprotsess toob kaasa mikrosüsteemi seisundi füüsikaliste parameetrite muutumise; selle muutuse alampiiri määrab samuti määramatuse seos.
Arvestades väiksust sama mõõtmega makroskoopiliste suurustega võrreldes, on määramatuse seoste mõjud olulised peamiselt aatomi- ja väiksema ulatusega nähtuste puhul ning makroskoopiliste kehadega tehtud katsetes ei ilmne.
Määramatuse suhted, mille sai esmakordselt 1927. aastal saksa füüsik W. Heisenberg, olid oluliseks sammuks aatomisiseste nähtuste mustrite selgitamisel ja kvantmehaanika ehitamisel.
Nagu lainefunktsiooni tähenduse statistilisest tõlgendamisest järeldub, saab osakest teatud tõenäosusega tuvastada igas ruumipunktis, kus lainefunktsioon on nullist erinev. Seetõttu on mõõtmiskatsete tulemused, näiteks koordinaadid, tõenäosuslikku laadi. See tähendab, et identsete süsteemide identsete katsete seeria läbiviimisel (st samade füüsikaliste tingimuste taasesitamisel) saadakse iga kord erinevad tulemused. Mõned väärtused on siiski tõenäolisemad kui teised ja ilmuvad sagedamini. Kõige sagedamini saadakse need koordinaatide väärtused, mis on lähedased väärtusele, mis määrab lainefunktsiooni maksimumi asukoha. Kui maksimum on selgelt väljendatud (lainefunktsioon on kitsas lainepakett), siis osake asub peamiselt selle maksimumi lähedal. Sellegipoolest on koordinaatide väärtuste mõningane hajumine (maksimumi poollaiuse järgu määramatus) vältimatu. Sama kehtib impulsi mõõtmise kohta.
Aatomisüsteemides on suurus suurusjärgus võrdne orbiidi pindalaga, mida mööda osake Bohr-Sommerfeldi teooria kohaselt faasitasandil liigub. Seda saab kontrollida, väljendades orbiidi pindala faasiintegraalis. Sel juhul selgub, et kvantarv (vt loeng 3) rahuldab tingimust
Erinevalt Bohri teooriast, kus toimub võrdsus (siin on elektronide kiirus esimesel Bohri orbiidil vesinikuaatomis, on valguse kiirus vaakumis), määratakse statsionaarsetes olekutes vaadeldaval juhul keskmine impulss süsteemi mõõtmed koordinaatruumis ja suhe on ainult suurusjärgus. Seega, kasutades mikroskoopiliste süsteemide kirjeldamiseks koordinaate ja impulssi, on vaja nende mõistete tõlgendamisse sisse viia kvantkorrektsioonid. Selline parandus on määramatuse seos.
Energia ja aja määramatuse suhtel on veidi erinev tähendus:
Kui süsteem on statsionaarses olekus, siis määramatuse seosest järeldub, et süsteemi energiat saab ka selles olekus mõõta ainult täpsusega, mis ei ületa seda, kus on mõõtmisprotsessi kestus. Seos (4.20) kehtib ka siis, kui mõistame suletud süsteemi mittestatsionaarse oleku energia väärtuse määramatust ja - iseloomulikku aega, mille jooksul füüsikaliste suuruste keskmised väärtused selles süsteemis oluliselt muutuvad. .
Määramatuse seos (4.20) viib oluliste järeldusteni aatomite, molekulide ja tuumade ergastatud olekute kohta. Sellised olekud on ebastabiilsed ja määramatuse seosest järeldub, et ergastatud tasandite energiaid ei saa täpselt määratleda, st energiatasemetel on teatud loomulik laius, kus on ergastatud oleku eluiga. Teine näide on radioaktiivse tuuma alfa-lagunemine. Emiteeritud -osakeste energia levik on seose kaudu seotud sellise tuuma elueaga.
Aatomi normaalse oleku jaoks on energial täpselt määratletud väärtus, see tähendab. Ebastabiilse osakese jaoks s, ja selle energia teatud väärtusest pole vaja rääkida. Kui aatomi eluiga ergastatud olekus võtta võrdseks c-ga, siis on energiataseme laius ~10 -26 J ja spektrijoone laius, mis tekib aatomi üleminekul normaalolekusse, ~10 8 Hz.
Määramatuse seostest järeldub, et koguenergia jagunemine kineetiliseks ja potentsiaalseks kaotab kvantmehaanikas oma tähenduse. Tõepoolest, üks neist sõltub momendist ja teine - koordinaatidest. Samadel muutujatel ei saa olla samal ajal teatud väärtusi. Energiat tuleks määratleda ja mõõta ainult koguenergiana, jagamata kineetiliseks ja potentsiaalseks energiaks.



