Что такое строение ядра атома. Состав и строение атомного ядра (кратко)
Атомное ядро
Atomic nucleus
Атомное ядро
– центральная и очень компактная часть атома, в которой сосредоточена практически
вся его масса и весь положительный электрический заряд. Ядро, удерживая
вблизи себя кулоновскими силами электроны в количестве, компенсирующем его
положительный заряд, образует нейтральный атом. Большинство ядер имеют форму
близкую к сферической и диаметр ≈ 10 -12 см, что на четыре порядка
меньше диаметра атома (10 -8 см). Плотность вещества в ядре –
около 230 млн.тонн/см 3 .
Атомное ядро было открыто в 1911 г. в результате серии экспериментов
по рассеянию альфа-частиц тонкими золотыми и платиновыми фольгами, выполненных
в Кембридже (Англия) под руководством
Э. Резерфорда .
В 1932 г. после открытия там же
Дж. Чедвиком
нейтрона стало ясно, что ядро состоит из протонов и нейтронов
(В.
Гейзенберг ,
Д.Д. Иваненко ,
Э. Майорана).
Для обозначения атомного ядра используется символ химического
элемента атома, в состав которого входит ядро, причём левый верхний индекс
этого символа показывает число нуклонов (массовое число) в данном ядре,
а левый нижний индекс – число протонов в нём. Например, ядро никеля, содержащее
58 нуклонов, из которых 28 протонов, обозначается
.
Это же ядро можно также обозначать 58 Ni, либо никель-58.
Ядро – система плотно упакованных протонов и нейтронов,
двигающихся со скоростью 10 9 -10 10 см/сек и удерживаемых
мощными и короткодействующими ядерными силами взаимного притяжения (область
их действия ограничена расстояниями ≈ 10 -13 см).
Протоны и нейтроны имеют размер около 10 -13 см и рассматриваются
как два разных состояния одной частицы, называемой нуклоном. Радиус ядра
можно приближённо оценить по формуле R ≈ (1.0-1.1)·10 -13 А 1/3
см, где А – число нуклонов (суммарное число протонов и нейтронов)
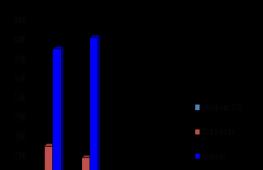
в ядре. На рис. 1 показано как меняется плотность
вещества (в
единицах 10 14 г/см 3) внутри ядра никеля, состоящего
из 28 протонов и 30 нейтронов, в зависимости от расстояния r (в единицах
10 -13 см) до центра ядра.
Ядерное взаимодействие (взаимодействие между нуклонами в ядре)
возникает за счёт того, что нуклоны обмениваются мезонами. Это взаимодействие
– проявление более фундаментального сильного взаимодействиямежду
кварками, из которых состоят нуклоны и мезоны (подобным образом силы химической
связи в молекулах – проявление более фундаментальных электромагнитных сил).
Мир ядер очень разнообразен. Известно около 3000 ядер, отличающихся
друг от друга либо числом протонов, либо числом нейтронов, либо тем и другим.
Большинство из них получено искусственным путём.
Лишь 264 ядра стабильны, т.е. не испытывают со временем никаких самопроизвольных
превращений, именуемых распадами. Остальные испытывают различные формы распада
– альфа-распад (испускание альфа-частицы, т.е. ядра атома гелия); бета-распад
(одновременное испускание – электрона и антинейтрино или позитрона и нейтрино,
а также поглощение атомарного электрона с испусканием нейтрино); гамма-распад
(испускание фотона) и другие.
Различные типы ядер часто называют нуклидами. Нуклиды с одинаковым
числом протонов и разным числом нейтронов называют изотопами. Нуклиды с
одинаковым числом нуклонов, но разным соотношением протонов и нейтронов
называются изобарами. Лёгкие ядра содержат примерно равные количества протонов
и нейтронов. У тяжёлых ядер число нейтронов примерно в 1,5 раза превышает
число протонов. Самое лёгкое ядро – ядро атома водорода, состоящее из одного
протона. У наиболее тяжелых известных ядер (они получены искусственно) число
нуклонов ≈290. Из них 116-118 протонов.
Различные комбинации количества протонов Z и нейтронов соответствуют
различным атомным ядрам. Атомные ядра существуют (т.е. их время жизни t
> 10 -23 c) в довольно узком диапазоне изменений чисел Z и N.
При этом все атомные ядра делятся на две большие группы - стабильные и радиоактивные
(нестабильные). Стабильные ядра группируются вблизи линии стабильности,
которая определяется уравнением
![]()
|
Рис. 2. NZ- диаграмма атомных ядер. |
На рис. 2 показана NZ-диаграмма атомных ядер. Черными
точками показаны стабильные ядра. Область расположения стабильных ядер обычно
называют долиной стабильности. С левой стороны от стабильных ядер находятся
ядра, перегруженные протонами (протонноизбыточные ядра), справа – ядра,
перегруженные нейтронами (нейтронноизбыточные ядра). Цветом выделены атомные
ядра, обнаруженные в настоящее время. Их около 3.5 тысяч. Считается, что
всего их должно быть 7 – 7.5 тысяч. Протоноизбыточные ядра (малиновый цвет)
являются радиоактивными и превращаются в стабильные в основном в результате
β + -распадов, протон, входящий в состав ядра при
этом превращается в нейтрон. Нейтроноизбыточные ядра (голубой цвет) также
являются радиоактивными и превращаются в стабильные в результате
- -распадов,
с превращением нейтрона ядра в протон.
Самыми тяжелыми стабильными изотопами являются изотопы свинца
(Z = 82) и висмута (Z = 83). Тяжелые ядра наряду с процессами β +
и β - -распада подвержены также α-распаду
(желтый цвет) и спонтанному делению, которые становятся их основными каналами
распада. Пунктирная линия на рис. 2 очерчивает область возможного существования
атомных ядер. Линия B p = 0 (B p – энергия
отделения протона) ограничивает область существования атомных ядер слева
(proton drip-line). Линия B n = 0 (B n – энергия отделения
нейтрона) – справа (neutron drip-line). Вне этих границ атомные ядра существовать
не могут, так как они распадаются за характерное ядерное время (~10 -23
– 10 -22 c) с испусканием нуклонов.
При соединении (синтезе) двух лёгких ядер и делении тяжёлого
ядра на два более лёгких осколка выделяется большая энергия. Эти два способа
получения энергии – самые эффективные из всех известных. Так 1 грамм ядерного
топлива эквивалентен 10 тоннам химического топлива. Синтез ядер (термоядерные
реакции) является источником энергии звёзд. Неуправляемый (взрывной) синтез
осуществляется при подрыве термоядерной (или, так называемой, “водородной”)
бомбы. Управляемый (медленный) синтез лежит в основе перспективного разрабатываемого
источника энергии – термоядерного реактора.
Неуправляемое (взрывное) деление происходит при взрыве атомной
бомбы. Управляемое деление осуществляется в ядерных реакторах, являющихся
источниками энергии в атомных электростанциях.
Для теоретического описания атомных ядер используется квантовая
механика и различные модели.
Ядро может вести себя и как газ (квантовый газ) и как жидкость
(квантовая жидкость). Холодная ядерная жидкость обладает свойствами сверхтекучести.
В сильно нагретом ядре происходит распад нуклонов на составляющие их кварки.
Эти кварки взаимодействуют обменом глюонами. В результате такого распада
совокупность нуклонов внутри ядра превращается в новое состояние материи
– кварк-глюонную плазму
СТРОЕНИЕ ЯДРА АТОМА
В 1932г. после открытия протона и нейтрона учеными Д.Д. Иваненко (СССР) и В. Гейзенберг (Германия) была выдвинута протонно-нейтронная модель ядра атома.
Согласно этой модели:
- ядра
всех химических элементов состоят из нуклонов
: протонов и нейтронов
- заряд ядра обусловлен только протонами
- число протонов в ядре равно порядковому номеру элемента
- число нейтронов равно разности между массовым числом и числом протонов (N=A-Z)
Условное обозначение ядра атома химического элемента:
X – символ химического элемента
А – массовое число
, которое показывает:
- массу ядра в целых атомных единицах массы (а.е.м.)
(1а.е.м. = 1/12 массы атома углерода)
- число нуклонов в ядре
- (A = N + Z) , где N – число нейтронов в ядре атома
Z – зарядовое число
, которое показывает:
- заряд ядра в элементарных электрических зарядах (э.э.з.)
(1э.э.з. = заряду электрона = 1,6 х 10 -19 Кл)
- число протонов
- число электронов в атоме
- порядковый номер в таблице Менделеева
Масса ядра всегда меньше
суммы масс покоя свободных протонов и нейтронов, его составляющих.
Это объясняется тем, что протоны и нейтроны в ядре очень сильно притягиваются друг к другу. Чтобы разъединить их требуется затратить большую работу. Поэтому полная энергия покоя ядра не равна энергии покоя составляющих его частиц. Она меньше на величину работы по преодолению ядерных сил притяжения.
Разность между массой ядра и суммой масс протонов и нейтронов называется дефектом масс.
Вспомни тему "Атомная физика" за 9 класс:
Радиоактивность.
Радиоактивные превращения.
Состав атомного ядра. Ядерные силы.
Энергия связи. Дефект масс.
Деление ядер урана.
Ядерная цепная реакция.
Ядерный реактор.
Термоядерная реакция.
Другие страницы по теме "Атомная физика" за 10-11 класс:
КАК ИЗУЧАЛИ АТОМ
Атом
– это ядро из протонов и нейтронов, вокруг которого вращаются электроны. Размеры атомов составляют тысячные доли микрона
. Но существуют и сверх гигантские «атомы»
диаметром около 10 километров. Впервые подобный «атом» был открыт в 1967 году, а сейчас их известно более тысячи. Это нейтронные звезды
– остатки сверхновых, которые являются фактически огромными атомными ядрами, состоящими на 90% из нейтронов и на 10% из протонов, и окружены «атмосферой» из электронов.
___
В 20-е годы один молодой физик проходил стажировку у Э. Резерфорда . Через два месяца Резерфорд пригласил его к себе и сообщил, что ничего не получится. "Почему? Ведь я работаю по 20 часов в сутки!?" - возразил молодой. "Это и плохо! У вас не остается времени на то, чтобы думать! » - ответил Резерфорд.
В 1908 году знаменитый физик Эрнест Резерфорд сказал, что он имел дело со многими превращениями в природе, но такое сиюминутное превращение ему вряд ли удалось бы предвидеть. – Из физиков в химики! В 1908 году Э. Резерфорд получил Нобелевскую премию по химии за свои работы в области изучения атома. В те годы исследования по строению атома и радиоактивности относили к химии.
Как уже отмечалось, атом состоит из трех видов элементарных частиц: протонов, нейтронов и электронов. Атомное ядро – центральная часть атома, состоящая из протонов и нейтронов. Протоны и нейтроны имеют общее название нуклон, в ядре они могут превращаться друг в друга. Ядро простейшего атома – атома водорода – состоит из одной элементарной частицы – протона.
Диаметр ядра атома равен примерно 10 -13 – 10 -12 см и составляет 0,0001 диаметра атома. Однако, практически вся масса атома (99,95 – 99,98 %) сосредоточена в ядре. Если бы удалось получить 1 см 3 чистого ядерного вещества, масса его составила бы 100 – 200 млн.т. Масса ядра атома в несколько тысяч раз превосходит массу всех входящих в состав атома электронов.
Протон – элементарная частица, ядро атома водорода. Масса протона равна 1,6721х10 -27 кг, она в 1836 раз больше массы электрона. Электрический заряд положителен и равен 1,66х10 -19 Кл. Кулон – единица электрического заряда, равная количеству электричества, проходящему через поперечное сечение проводника за время 1с при неизменной силе тока 1А (ампер).
Каждый атом любого элемента содержит в ядре определенное число протонов. Это число постоянное для данного элемента и определяет его физические и химические свойства. То есть, от количества протонов зависит, с каким химическим элементом мы имеем дело. Например, если в ядре один протон – это водород, если 26 протонов – это железо. Число протонов в атомном ядре определяет заряд ядра (зарядовое число Z) и порядковый номер элемента в периодической системе элементов Д.И. Менделеева (атомный номер элемента).
Н ейтрон – электрически нейтральная частица с массой 1,6749 х10 -27 кг, в 1839 раз больше массы электрона. Нейрон в свободном состоянии – нестабильная частица, он самостоятельно превращается в протон с испусканием электрона и антинейтрино. Период полураспада нейтронов (время, в течение которого распадается половина первоначального количества нейтронов) равен примерно 12 мин. Однако в связанном состоянии внутри стабильных атомных ядер он стабилен. Общее число нуклонов (протонов и нейтронов) в ядре называют массовым числом (атомной массой – А). Число нейтронов, входящих в состав ядра, равно разности между массовым и зарядовым числами: N = A – Z.
Электрон – элементарная частица, носитель наименьшей массы – 0,91095х10 -27 г и наименьшего электрического заряда – 1,6021х10 -19 Кл. Это отрицательно заряженная частица. Число электронов в атоме равно числу протонов в ядре, т.е. атом электрически нейтрален.
Позитрон – элементарная частица с положительным электрическим зарядом, античастица по отношению к электрону. Масса электрона и позитрона равны, а электрические заряды равны по абсолютной величине, но противоположны по знаку.
Различные типы ядер называют нуклидами. Нуклид – вид атомов с данными числами протонов и нейтронов. В природе существуют атомы одного и того же элемента с разной атомной массой (массовым числом): 17 35 Cl, 17 37 Cl и т.д. Ядра этих атомов содержат одинаковое число протонов, но различное число нейтронов. Разновидности атомов одного и того же элемента, имеющие одинаковый заряд ядер, но различное массовое число, называются изотопами . Обладая одинаковым количеством протонов, но различаясь числом нейтронов, изотопы имеют одинаковое строение электронных оболочек, т.е. очень близкие химические свойства и занимают одно и то же место в периодической системе химических элементов.
Изотопы обозначают символом соответствующего химического элемента с расположенным сверху слева индексом А – массовым числом, иногда слева внизу приводится также число протонов (Z). Например, радиоактивные изотопы фосфора обозначают 32 Р, 33 Р или 15 32 Р и 15 33 Р соответственно. При обозначении изотопа без указания символа элемента массовое число приводится после обозначения элемента, например, фосфор – 32, фосфор – 33.
Большинство химических элементов имеет по несколько изотопов. Кроме изотопа водорода 1 Н-протия, известен тяжелый водород 2 Н-дейтерий и сверхтяжелый водород 3 Н-тритий. У урана 11 изотопов, в природных соединениях их три (уран 238, уран 235, уран 233). У них по 92 протона и соответственно 146,143 и 141 нейтрон.
В настоящее время известно более 1900 изотопов 108 химических элементов. Из них к естественным относятся все стабильные (их примерно 280) и естественные изотопы, входящие в состав радиоактивных семейств (их 46). Остальные относятся к искусственным, они получены искусственным путем в результате различных ядерных реакций.
Термин «изотопы» следует применять только в тех случаях, когда речь идет об атомах одного и того же элемента, например, изотопы углерода 12 С и 14 С. Если подразумеваются атомы разных химических элементов, рекомендуется использовать термин «нуклиды», например, радионуклиды 90 Sr, 131 J, 137 Cs.
Атомное ядро — это центральная часть атома, состоящая из протонов и нейтронов (которые вместе называются нуклонами ).
Ядро было открыто Э. Резерфордом в 1911 г. при исследовании прохождения α -частиц через вещество. Оказалось, что почти вся масса атома (99,95%) сосредоточена в ядре. Размер атомного ядра имеет порядок величины 10 -1 3 -10 - 12 см, что в 10 000 раз меньше размера электронной оболочки.
Предложенная Э. Резерфордом планетарная модель атома и экспериментальное наблюдение им ядер водорода , выбитых α -частицами из ядер других элементов (1919-1920 гг.), привели уче-ного к представлению о протоне . Термин протон был введен в начале 20-х гг XX ст.
Протон (от греч. protons — первый, символ p ) — стабильная элементарная частица, ядро ато-ма водорода.
Протон — положительно заряженная частица, заряд которой по абсолютной величине равен заряду электрона e = 1,6 · 10 -1 9 Кл. Масса протона в 1836 раз больше массы электрона. Масса покоя протона m р = 1,6726231 · 10 -27 кг = 1,007276470 а.е.м.
Второй частицей, входящей в состав ядра, является нейтрон .
Нейтрон (от лат. neuter — ни тот, ви другой, символ n ) — это эле-ментарная частица, не имеющая заряда, т. е. нейтральная.
Масса нейтрона в 1839 раз превышает массу электрона. Масса нейтрона почти равна (незначительно больше) массе протона: масса покоя свободного нейтрона m n = 1,6749286 · 10 -27 кг = 1,0008664902 а.е.м. и превосходит массу протона па 2,5 массы электрона. Нейтрон, наря-ду с протоном под общим названием нуклон входит в состав атомных ядер.
Нейтрон был открыт в 1932 г. учеником Э. Резерфорда Д. Чедвигом при бомбардировке бериллия α -частицами. Возникающее при этом излучение с большой проникающей способностью (преодолевало пре-граду из свинцовой пластины толщиной 10-20 см) усиливало свое действие при прохождении через парафиновую пластину (см. рисунок). Оценка энергии этих частиц по трекам в камере Вильсона, сделанная супругами Жолио-Кюри, и дополнительные наблюдения позволили исключить первоначальное предположение о том, что это γ -кванты. Большая проникающая способность новых частиц, названных ней-тронами, объяснялась их электронейтральностью. Ведь заряженные частицы активно взаимодействуют с веществом и быстро теряют свою энергию. Существование нейтронов было предсказано Э. Резерфордом за 10 лет до опытов Д. Чедвига. При попадании α -частиц в ядра бериллия происходит следующая реакция:
Здесь — символ нейтрона; заряд его равен нулю, а относительная атомная масса прибли-зительно равна единице. Нейтрон — нестабильная частица: свободный нейтрон за время ~ 15 мин. распадается на протон, электрон и нейтрино — частицу, лишенную массы покоя.
После открытия Дж. Чедвиком нейтрона в 1932 г. Д. Иваненко и В. Гейзенберг независимо друг от друга предложили протонно-нейтронную (нуклонную) модель ядра . Согласно этой моде-ли, ядро состоит из протонов и нейтронов. Число протонов Z совпадает с порядковым номером элемента в таблице Д. И. Менделеева .
Заряд ядра Q определяется числом протонов Z , входящих в состав ядра, и кратен абсолютной величине заряда электрона e :
Q = +Ze.
Число Z называется зарядовым числом ядра или атомным номером .
Массовым числом ядра А называется общее число нуклонов, т. е. протонов и нейтронов, содер-жащихся в нем. Число нейтронов в ядре обозначается буквой N . Таким образом, массовое число равно:
А = Z + N.
Нуклонам (протону и нейтрону) приписывается массовое число, равное единице, электрону — нулевое значение.
Представлению о составе ядра содействовало также открытие изотопов .
Изотопы (от греч. isos — равный, одинаковый и topoa — место) — это разновидности атомов одного и того же химического элемента, атомные ядра которых имеют одинаковое число прото-нов (Z ) и различное число нейтронов (N ).
Изотопами называются также ядра таких атомов. Изотопы являются нуклидами одного эле-мента. Нуклид (от лат. nucleus — ядро) — любое атомное ядро (соответственно атом) с заданными числами Z и N . Общее обозначение нуклидов имеет вид ……. где X — символ химического эле-мента, A = Z + N — массовое число.
Изотопы занимают одно и то же место в Периодической системе элементов, откуда и про-изошло их название. По своим ядерным свойствам (например, по способности вступать в ядерные реакции) изотопы, как правило, существенно отличаются. Химические (b почти в той же мере физические) свойства изотопов одинаковы. Это объясняется тем, что химические свойства элемен-та определяются зарядом ядра, поскольку именно он влияет на структуру электронной оболочки атома.
Исключением являются изотопы легких элементов. Изотопы водорода 1 Н — протий , 2 Н — дейтерий , 3 Н — тритий столь сильно отличаются по массе, что и их физические и хими-ческие свойства различны. Дейтерий стабилен (т.е. не радиоактивен) и входит в качестве неболь-шой примеси (1: 4500) в обычный водород. При соединении дейтерия с кислородом образуется тяжелая вода . Она при нормальном атмосферном давлении кипит при 101,2 °С и замерзает при +3,8 ºС. Тритий β -радиоактивен с периодом полураспада около 12 лет.
У всех химических элементов имеются изотопы. У некоторых элементов имеются только нестабильные (радиоактивные) изотопы. Для всех элементов искусственно получены радиоактив-ные изотопы.
Изотопы урана. У элемента урана есть два изотопа — с массовыми числами 235 и 238. Изотоп составляет всего 1/140 часть от более распространенного .
>> Строение атомного ядра. Ядерные силы
§ 104 СТРОЕНИЕ АТОМНОГО ЯДРА. ЯДЕРНЫЕ СИЛЫ
Сразу же после того, как в опытах Чедвика был открыт нейтрон , советский физик Д. Д. Иваненко и немецкий ученый В. Гейзенберг в 1932 г. предложили протонно-нейтронную модель ядра. Она была подтверждена последующими исследованиями ядерных превращений и в настоящее время является общепризнанной.
Протонно-нейтронная модель ядра. Согласно протонно-нейтронной модели ядра состоят из элементарных частиц двух видов - протонов и нейтронов.
Так как в целом атом электрически нейтрален, а заряд протона равен модулю заряда э-иектрона, то число протонов в ядре равно числу электронов в атомной оболочке. Следовательно, число протонов в ядре равно атомному номеру элемента Z в периодической системе элементов Д. И. Менделеева .
Сумму числа протонов Z и числа нейтронов N в ядре называют массовым числом и обозначают буквой А:
А = Z + N. (13.2)
Массы протона и нейтрона близки друг к другу, и каждая из них примерно равна атомной единице массы. Масса электронов в атоме много меньше массы его ядра. Поэтому массовое число ядра равно округленной до целого числа относительной атомной массе элемента. Массовые числа могут быть определены путем приближенного измерения массы ядер приборами, не обладающими высокой точностью.
Изотопы представляют собой ядра с одним и тем же значением но с различными массовыми числами А, т. е. с различными числами нейтронов N.
Ядерные силы. Так как ядра весьма устойчивы, то протоны и нейтроны должны удерживаться внутри ядра какими-то силами, причем очень большими. Что это за силы? Сразу можно сказать, что это не гравитационные силы, которые слишком слабые. Устойчивость ядра не может быть объяснена также электромагнитными силами, так как между одноименно заряженными протонами действует электрическое отталкивание. А нейтроны не имеют электрического заряда.
Значит, между ядерными частицами - протонами и нейтронами (их называют нуклонами) - действуют особые силы, называемые ядерными силами.
Каковы основные свойства ядерных сил? Ядерные силы примерно в 100 раз превышают электрические (кулоновские) силы. Это самые мощные силы из всех сущес;гнующих в природе. Поэтому взаимодействия ядерных частиц часто называют сильными взаимодействиями.
Сильные взаимодействия проявляются не только во взаимодействиях нуклонов в ядре . Это особый тип взаимодействий, присущий большинству элементарных частиц наряду с электромагнитными взаимодействиями.
Другая важная особенность ядерных сил - их коротко-действие. Электромагнитные силы сравнительно медленно ослабевают с увеличением расстояния. Ядерные силы заметно проявляются лишь на расстояниях, равных размерам ядра (10 -12 -10 -13 см), что показали уже опыты Резерфорда по рассеянию -частиц атомными ядрами. Ядерные силы - это, так сказать, «богатырь с очень короткими руками». Законченная количественная теория ядерных сил пока еще не разработана. Значительные успехи в ее разработке были достигнуты совсем недавно - в последние 10-15 лет.
Ядра атомов состоят из протонов и нейтронов. Эти частицы удерживаются в ядре ядерными силами.
Каковы главные особенности ядерных сил!
Содержание урока конспект урока опорный каркас презентация урока акселеративные методы интерактивные технологии Практика задачи и упражнения самопроверка практикумы, тренинги, кейсы, квесты домашние задания дискуссионные вопросы риторические вопросы от учеников Иллюстрации аудио-, видеоклипы и мультимедиа фотографии, картинки графики, таблицы, схемы юмор, анекдоты, приколы, комиксы притчи, поговорки, кроссворды, цитаты Дополнения рефераты статьи фишки для любознательных шпаргалки учебники основные и дополнительные словарь терминов прочие Совершенствование учебников и уроков исправление ошибок в учебнике обновление фрагмента в учебнике элементы новаторства на уроке замена устаревших знаний новыми Только для учителей идеальные уроки календарный план на год методические рекомендации программы обсуждения Интегрированные уроки